El valor más grande de un profesional es su potencial de hacer la diferencia y usarlo para sumar en su ámbito de acción.
Autora: Lourdes Molina, 08 de septiembre del 2025
El mantenimiento del Certificado de Cumplimiento de Buenas Prácticas de Fabricación coloquialmente llamado GMP es un desafío constante para las plantas locales de fabricación de fármacos, medicamentos y dispositivos médicos. Los desafíos más importantes son:
- El cumplimiento sostenido del marco normativo aplicable.
- Disponibilidad de la evidencia para solicitar la prórroga del GMP con una anticipación de seis meses antes del vencimiento de este.
- El tiempo que tarda la COFEPRIS en programar la visita de verificación, que en promedio es de siete meses, aunque el plazo puede ser más corto o largo. Esto implica que, aunque la visita se pida con seis meses de anticipación, el riesgo de tener un GMP vencido es alto.
- El tiempo que tarda la COFEPRIS en otorgar el GMP renovado, aunque COFEPRIS lo considera válido si ya se venció, pero se cuenta con evidencia de que ya se llevó a cabo la visita de verificación en forma satisfactoria y el trámite está en curso.
Lo anterior sin mencionar el impacto de un GMP local vencido, en los siguientes procesos:
- Registro sanitario de medicamentos y dispositivos médicos.
- Renovación de registros sanitarios.
- Reconocimiento internacional, es decir, se entorpece la renovación del GMP, en países que consideran el GMP de México como equivalente.
- Licitación pública de medicamentos y dispositivos médicos.
Por otro lado, contar con un GMP local vigente ofrece ventajas importantes:
- Agiliza la evaluación del dossier de registro o prórroga, pues el fabricante demuestra que cumple con los estándares de calidad sin necesidad de inspecciones regulatorias adicionales.
- El GMP otorgado por COFEPRIS es considerado equivalente en Centroamérica y Caribe, entre otros. Por lo anterior, se reduce el tiempo y costo de registro de medicamentos y dispositivos médicos en una forma importante.
- Califica a las plantas locales de las empresas que participan en licitaciones públicas ya que, es un requisito técnico por cumplir para poder participar.
- Otorga puntaje adicional en las licitaciones públicas a las empresas que cuentan con planta en México certificada por COFEPRIS.
- Califica a las plantas locales de las empresas para licitaciones internacionales como las de la OPS.
- Les otorga un posicionamiento competitivo y de confianza ante COFEPRIS y otras agencias regulatorias, cuando cuentan con un largo historial de cumplimiento.

El mantenimiento del GMP de las plantas locales involucra muchos desafíos, entre los que quiero mencionar algunos:
- Falta de madurez del Sistema de Gestión de Calidad.
- Rotación de personal.
- Liquidez de capital.
- Modificación constante del portafolio de productos.
- Desconocimiento de la regulación aplicable al producto, a la planta, a los procesos de distribución y dispensación.
- Falta de involucramiento en los proyectos de lanzamiento de nuevos productos. por parte del equipo de planta.
- Modificaciones regulatorias con impacto en los procesos y productos.
- Inadecuada calificación y gestión de proveedores.
- Inadecuada gestión de los clientes involucrados en la cadena de abasto.
- Sostenibilidad del abasto del canal.
- La revisión por la dirección.
De cada uno de estos podemos hablar en una forma basta pero cada uno de ustedes queridos lectores, sabe lo que le duele a su planta y a su cadena de suministro en general. Entonces me quiero centrar en un tema que es la piedra angular para lograr que todo funcione en forma sincronizada, el sistema de gestión de calidad.
El sistema de gestión de calidad óptimo transforma en forma sutil y progresiva a los colaboradores de una empresa farmacéutica que opera con planta ya que, forma una cultura de calidad con un enfoque genuino al paciente. La operación óptima del sistema de gestión de calidad se logra cuando todos los colaboradores realizan sus funciones y evalúan los eventos para tomar decisiones con un enfoque de riesgo.
Un sistema de gestión de calidad óptimo es difícil de encontrar en México y en el mundo porque es desarrollado e implementado en una forma rígida y compleja que aumenta en forma importante la carga administrativa a los colaboradores, quienes en su afán para superar las situaciones terminan por convertir al sistema de gestión de calidad en una ventanilla de trámites, perdiendo de vista la gran potencia del sistema para lograr la mejora continua y sustentable.
Otro factor muy importante que traer a la atención es el alcance del sistema de gestión de calidad. En general, el alcance es a la planta y a los procesos de distribución ya que, el espíritu del sistema de calidad es lograr que el medicamento o dispositivo médico esté disponible en el momento en que un paciente lo necesita. Sin embargo, los procesos de desarrollo de nuevos negocios, asuntos regulatorios, asuntos médicos, marketing y ventas usualmente están fuera del alcance del sistema de gestión de calidad, a pesar de que, forman parte de la cadena de suministro debido a que realizan funciones que contribuyen a generar oportunidades de acceso a medicamentos y dispositivos médicos, así como, a mantener el abasto del canal.
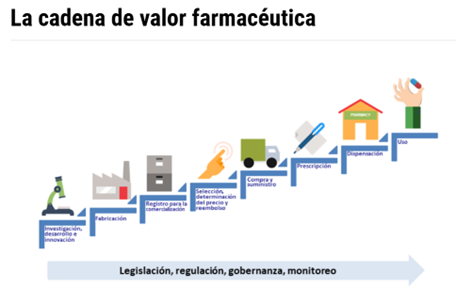
En suma cada uno de los eslabones de la cadena de suministro deben interactuar con los diferentes elementos del sistema de gestión de calidad, lo que implica una extensión hacia los proveedores y a los clientes, es decir, los distribuidores y mayoristas, farmacias hospitalarias y farmacias independientes o de cadena y los procesos de dispensación al paciente, aunque estos, son monitoreados a través de la Farmacovigilancia y Tecnovigilancia, que también debe de tener una coyuntura con los diferentes elementos del sistema de gestión de calidad.
Me gustaría dejarles una pregunta para reflexionar a todos ustedes queridos lectores: ¿Qué impacto tiene el sistema de gestión de calidad en el mantenimiento del GMP y en el abasto del canal?
Estaré al pendiente de sus comentarios ya que, los tomaré en cuenta para desarrollar las partes 2, 3 y 4 de este tema tan rico y que ofrece más posibilidades de las que podemos apreciar. Una de las posibilidades es plantear una propuesta para lograr optimizaciones que confluyan en la sostenibilidad del GMP y del abasto del canal para lograr un mayor acceso de insumos con un mejor balance costo beneficio.
Finalmente queremos invitarles a formar parte del grupo de trabajo que hemos formado en AMEPRES para desarrollar una propuesta enfocada a lograr la sostenibilidad del GMP y el abasto sostenible del canal. Afíliate a AMEPRES y pregunta sobre nuestra mesa de trabajo. ¡Te esperamos!
