El valor más grande de un profesional es su potencial de hacer la diferencia y usarlo para sumar en su ámbito de acción.
Autora: Lourdes Molina, 01 AGO 2025
Introducción:
El Reliance Farmacéutico en México ha tenido una evolución paulatina que ha involucrado grandes esfuerzos de COFEPRIS para generar acuerdos de equivalencia unilaterales fundadas en la confianza de que otras agencias sanitarias se apeguen a la Buenas Prácticas Regulatorias dictadas por la OMS. De acuerdo con lo anterior, este artículo muestra una recapitulación de la evolución del Reliance Farmacéutico en México.
Desarrollo:
El reconocimiento de las decisiones tomadas por otras agencias sanitarias tuvo sus orígenes en un acuerdo publicado en el 2010, que fue motivado por la eliminación del requisito de planta en ese mismo año. De acuerdo con la publicación, los aspectos considerados para emitir acuerdos de equivalencia son:
- Analizar los requisitos de evaluación técnica y científica que las entidades sanitarias extranjeras solicitan para permitir la comercialización de insumos para la salud en su país.
- Analizar los procedimientos de evaluación técnica y científica que las entidades sanitarias extranjeras llevan a cabo para garantizar la calidad, seguridad y eficacia de los insumos para la salud.
- Analizar los mecanismos y controles necesarios de farmacovigilancia y tecnovigilancia que realizan las entidades sanitarias extranjeras.
- Analizar la experiencia de comercialización de insumos para la salud cuyos registros sanitarios fueron otorgados por entidades sanitarias extranjeras.
- Que todos puntos anteriores, otorguen certeza sobre la seguridad, calidad y eficacia de los insumos en el mismo grado o en mayor grado, que el que otorgan los requisitos, pruebas, procedimientos de evaluación y requerimientos solicitados por la COFEPRIS.
Los aspectos antes mencionados son el fundamento del artículo 161 bis del Reglamento de Insumos para la salud, que a la letra dice: “La secretaría podrá expedir disposiciones de carácter general que tengan por objeto reconocer que los requisitos, pruebas, procedimientos de evaluación y demás requerimientos solicitados por las autoridades sanitarias extranjeras para permitir en sus respectivos países, la venta, distribución y uso de insumos a que se refiere este Reglamento, son equivalentes a los que la Ley, el presente Reglamento y demás disposiciones aplicables exigen para garantizar la calidad, seguridad y eficacia que deben satisfacer dichos insumos para obtener su registro sanitario en el país”.
Conforme a lo anterior, en el 2011, COFEPRIS implementó los carriles rápidos para solicitudes de registro de Dispositivos Médicos por equivalencia con FDA y Health Canada a propósito de:
- Implementar procedimientos abreviados de evaluación aplicables a los carriles rápidos.
- Reducir el rezago en la evaluación de registros sanitarios.
- Acelerar el acceso a insumos esenciales.
- Establecer confianza regulatoria en agencias internacionales.
En el 2012 se sumaron a los carriles rápidos las solicitudes de registro sanitario de Dispositivos Médicos por equivalencia con EMA (Europa) y PMDA (Japón).
En el 2020 se aceptan por primera vez los registros sanitarios por equivalencia de medicamentos a causa de la pandemia por Covid 19. En este caso las agencias reconocidas eran FDA, Health Canada, EMA, TGA, Agencia Suiza de Medicamentos, Miembros del PIC/S y la Agencias Reguladoras de referencia de OMS/OPS, así como, los medicamentos sujetos al programa de precalificación para medicamentos y vacunas de la Organización Mundial de la Salud. En tiempos de pandemia, la COFEPRIS generó una serie de acciones adaptativas para poder tener abasto de medicamentos y dispositivos médicos, a fin de, hacer frente a la emergencia sanitaria. Entre otras cosas nació la Autorización para Uso de Emergencia que al parecer llegó para quedarse, ya que aplica al registro de vacunas con tecnologías de ARNm que evolucionan con las variantes de los virus, como es el caso de la vacuna contra Covid 19.
A partir del 2020 ha habido múltiples cambios en los que se han sumado agencias regulatorias reconocidas por COFEPRIS, lo que ha dado lugar al registro sanitario de innumerables insumos para la salud provenientes del extranjero lo que ha generado una carga administrativa a la agencia reguladora local de tal magnitud, que no le ha sido posible cumplir con el tiempo de 60 días para la obtención del registro sanitario por equivalencias. Cabe mencionar, que los acuerdos de equivalencia no son vinculatorios, esto quiere decir que el hecho de que COFEPRIS reconozca el registro otorgado por otra agencia no implica que otorgará un registro sanitario en automático, ni que eximirá al titular del registro de cumplir con los requerimientos normativos locales.
Estos cambios tuvieron un gran impacto colateral que derivaron en modificaciones a diferentes Normas Oficiales Mexicanas como se lista a continuación:

En cuanto al formato del dossier de registro, en julio del 2024, la COFEPRIS publicó por primera vez una guía para estructurar el expediente conforme al Documento Técnico Común (CTD).
También se han hecho múltiples modificaciones a los criterios para reconocer el Certificado de Buenas Prácticas de Fabricación que acompaña el registro sanitario siendo que el más reciente fue publicado en marzo del 2025. En este mismo mes se publicaron los criterios para la autorización de Protocolos de Investigación en seres humanos que cuenten con la autorización previa por Autoridad Regulatoria Extranjera aplicable a protocolos de estudios clínicos fase III. En este caso, si el protocolo cumple los criterios, el plazo de autorización es de 45 días.
Todos estos cambios han sido enfocados a una alineación paulatina con los estándares internacionales entre los que más destacan las guías de la ICH, las Buenas Prácticas Regulatorias de la OMS y otros compromisos internacionales sujetos al programa de mejora regulatoria adscrita a la Ley General de Mejora Regulatoria.
En junio del 2025 se publicó el acuerdo de equivalencias en el que están indicados los criterios para para la importación de insumos que tienen el propósito de atender enfermedades emergentes, desatendidas o en casos de emergencia nacional al incrementar el acceso de medicamentos a la población mexicana, mediante el reconocimiento de las decisiones de otras agencias regulatorias de referencia (Reliance).
Finalmente, el 18 de julio del 2025, la COFEPRIS publicó: el ACUERDO por el que se emiten los Lineamientos generales para la aplicación de la vía regulatoria abreviada para el otorgamiento de los registros sanitarios de insumos para la salud en los que se reconocen como equivalentes los requisitos solicitados, pruebas y procedimientos de evaluación emitidos por autoridades regulatorias de referencia y el programa de precalificación de la Organización Mundial de la Salud. Este documento deja sin efecto todos los acuerdos de equivalencia publicados desde el 2010 y establece los lineamientos para aplicación de la vía regulatoria abreviada para el otorgamiento de los registros sanitarios de Insumos para la Salud en los que se reconocen como equivalentes los requisitos solicitados, pruebas y procedimientos de evaluación emitidos por Autoridades Regulatorias de Referencia y el programa de precalificación de la Organización Mundial de la Salud. Este acuerdo entra en vigor el 29 de agosto del 2025.
Cabe mencionar que estos lineamientos son aplicables a:
- Medicamentos (moléculas nuevas, genéricos, biotecnológicos innovadores y biocomparables, así como a, productos biológicos y vacunas).
- Dispositivos Médicos.
Otro dato importante por destacar es que el reconocimiento sólo es aplicable si se presenta la autorización obtenida por vía ordinaria por parte de la agencia reconocida. Por lo anterior, no aplican estos lineamientos para solicitudes fundadas en:
Las evaluaciones obtenidas por mecanismos Reliance;
I. Reconocimiento;
III. Aprobación acelerada;
IV. Aprobación condicionada;
V. Autorización por emergencia;
VI. Aprobación por orden judicial; y,
VII. Cualquier otro esquema de evaluación diferente a la vía de aprobación ordinaria.
En el lineamiento también se mencionan las ARR (Autoridades Reguladoras de Referencia) que reconoce la COFEPRIS en cuanto a sus decisiones regulatorias para el registro de medicamentos y dispositivos médicos.
De acuerdo con lo anterior, las ARR reconocidas para el registro de medicamentos son:
- Miembros fundadores ICH o miembros reguladores permanentes; y
- Agencias Regulatorias incluidas en el listado de WLA (con la función “Autorización de registro y comercialización” para medicamentos).
Para medicamentos genéricos, adicional a las ARR anteriormente mencionadas, se podrán utilizar las evaluaciones realizadas por la OMS, a través de su Programa de Precalificación de Medicamentos.
Para Dispositivos Médicos, la COFEPRIS reconoce las decisiones de autoridades reguladoras de referencia de:
- Países miembros del Management Committee del International Medical Device Regulators Forum (IMDRF)
- Miembros plenos del Programa de Auditoría Única de Dispositivos Médicos (MDSAP por sus siglas en inglés), para Certificados de Buenas Prácticas de Fabricación.
El lineamiento también menciona las homoclaves para solicitar registros sanitarios por equivalencia con ARR. En la tabla se incluyen los detalles de las homoclaves y de los plazos para obtener el registro sanitario.
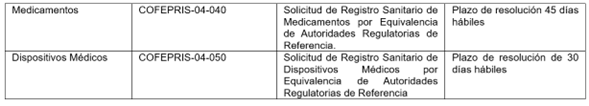
Para la vía abreviada de registro, los trámites deben ser presentados en formato CTD y conforme lo indicado en el lineamiento en comento.
Finalmente, todos estos esfuerzos para poder aplicar los acuerdos de equivalencia han sido acompañados por acuerdos de simplificación de trámites que han sido continuamente publicados desde el 2022. La simplificación de trámites permite bajar la carga administrativa a la agencia y facilitar el proceso de digitalización de trámites que están ocurriendo en forma paralela. Cabe mencionar que, a partir de esta administración presidencial, estos esfuerzos están vinculados al Plan México emitido en abril del 2025 en el que se incluyen acciones para la simplificación y digitalización de trámites.
Conclusiones:
Esta recapitulación nos lleva a estar conscientes de que todas las iniciativas publicadas están dirigidas a la eficacia y competitividad regulatoria. Sin embargo, su correcta instrumentación es la clave del éxito. En este caso, la asignación del presupuesto adecuado y el engrosamiento de las filas de la COFEPRIS, con funcionarios bien calificados, es fundamental.
Es importante destacar que los trámites abreviados y la aplicación de los acuerdos de Reliance, son punta de lanza para garantizar el acceso de insumos para la salud a la población mexicana y al mismo tiempo abren la oportunidad de acunar inversiones locales y extranjeras en proyectos de innovación y desarrollo farmacéutico.
